腫瘤球或微腫瘤是重要的三維體外腫瘤模型,與二維細(xì)胞培養(yǎng)相比,它們與腫瘤在體內(nèi)的“微環(huán)境”極為相似。微腫瘤在基礎(chǔ)癌癥研究、藥物發(fā)現(xiàn)和精準(zhǔn)醫(yī)學(xué)等領(lǐng)域得到了廣泛應(yīng)用。在精準(zhǔn)醫(yī)學(xué)中,源自患者腫瘤細(xì)胞的腫瘤球體為藥物敏感性和耐藥性測試提供了一種有前景的系統(tǒng)。已建立的基于 96 和 384 孔微孔板的細(xì)胞球體常規(guī)篩選平臺需要相對較多的細(xì)胞和化合物,并且每個培養(yǎng)皿中往往會形成多個球體。本研究展示了基于親水-超疏水圖案化技術(shù)的微滴陣列平臺與懸滴法相結(jié)合的應(yīng)用,用于構(gòu)建高度微型化的單球體微陣列。以幾種常用的癌細(xì)胞系開始,在 100 nL ,含 150 個細(xì)胞的微滴中培養(yǎng),24 至 48 小時內(nèi)即可形成球體。該方法具有潛在應(yīng)用價值,可用于 3D 癌癥球體或微腫瘤的高通量化合物篩選,這對于基礎(chǔ)癌癥研究、藥物發(fā)現(xiàn)和精準(zhǔn)醫(yī)學(xué)領(lǐng)域至關(guān)重要。
本研究所用DMA玻片為經(jīng)過親水與超疏水處理的玻璃玻片。親水位點被超疏水區(qū)域間隔開。玻片為25 X 75 mm,包含588個邊長為1 mm的親水位點(圖2A、B)。
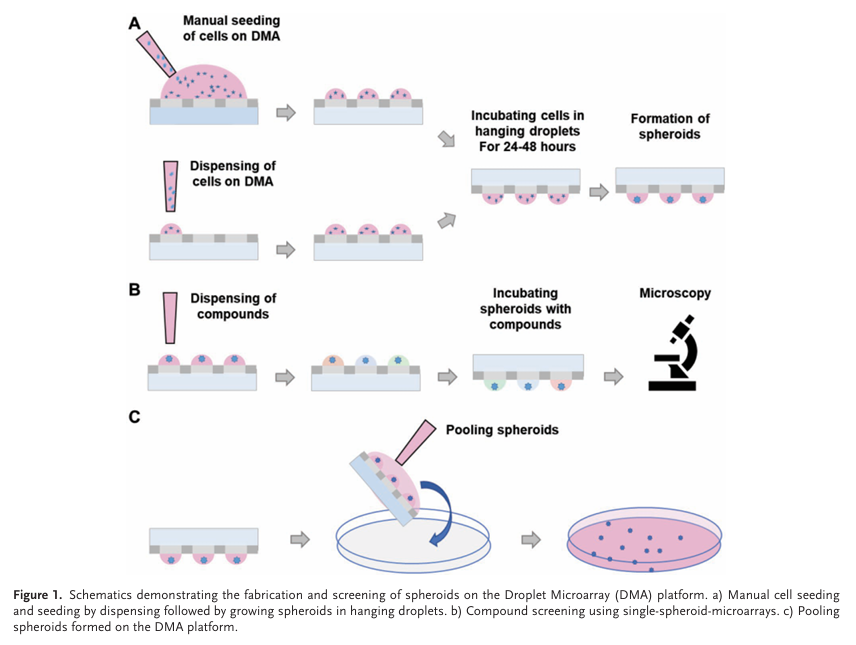
在此,我們同時采用了不連續(xù)的去濕技術(shù)(圖 1A上半部分)和非接觸式噴頭來將細(xì)胞直接打印到每個親水性點上(圖 1A下半部分)。如果是手動種細(xì)胞,細(xì)胞會被置于約 80 納升的液滴中,如果是使用機(jī)器接種,細(xì)胞會被置于 100 納升的液滴中。細(xì)胞接種完成后,將 DMA 玻片翻轉(zhuǎn)過來并放置在載玻片支架上,以形成懸掛液滴陣列(圖 1A和 2B)。帶有 DMA 玻片的載玻片支架被放入一個裝有緩沖液的 10 厘米培養(yǎng)皿中,并用含有濕潤墊的蓋子封閉,在標(biāo)準(zhǔn)細(xì)胞培養(yǎng)箱中進(jìn)行培養(yǎng),防止培養(yǎng)過程中液滴的蒸發(fā)。24-48小時后即可形成單球陣列(圖2C、D)。這種單細(xì)胞球體陣列可用于進(jìn)行復(fù)合操作,在 DMA 玻片上直接進(jìn)行顯微鏡分析,每個球體都可以單獨進(jìn)行定位(圖 1B)。此外,還可以通過將球體從無壁表面沖洗至培養(yǎng)皿或其他容器中來輕松收集它們,以便進(jìn)行進(jìn)一步的實驗或分析(圖 1C)。因此,DMA 技術(shù)不僅可以作為球體篩選的平臺,還可以作為制造數(shù)百個均勻單球體的平臺,這些單球體還可用于各種應(yīng)用。
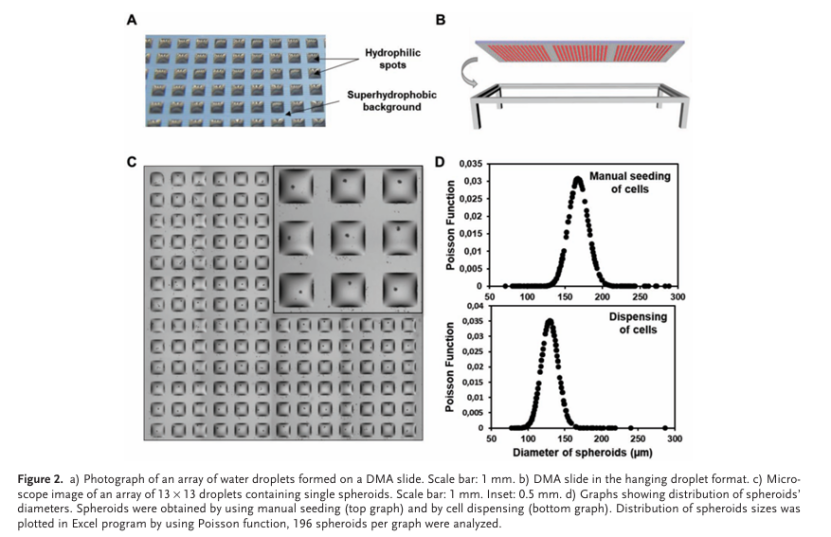
我們成功地從多種細(xì)胞類型(包括 MCF-7、HEK293 和 HeLa 細(xì)胞)中形成了球體(圖 2C 和 3)。
形成的球體在陣列中的大小分布與泊松分布相符,直徑偏差約為 14%,且兩種手動和自動接種方法的結(jié)果相當(dāng)(圖 2D)。在手動和自動接種方法中(圖 2D)。球體的大小取決于液滴中初始細(xì)胞的數(shù)量,并且可以通過改變初始細(xì)胞接種濃度來控制(圖 3C)
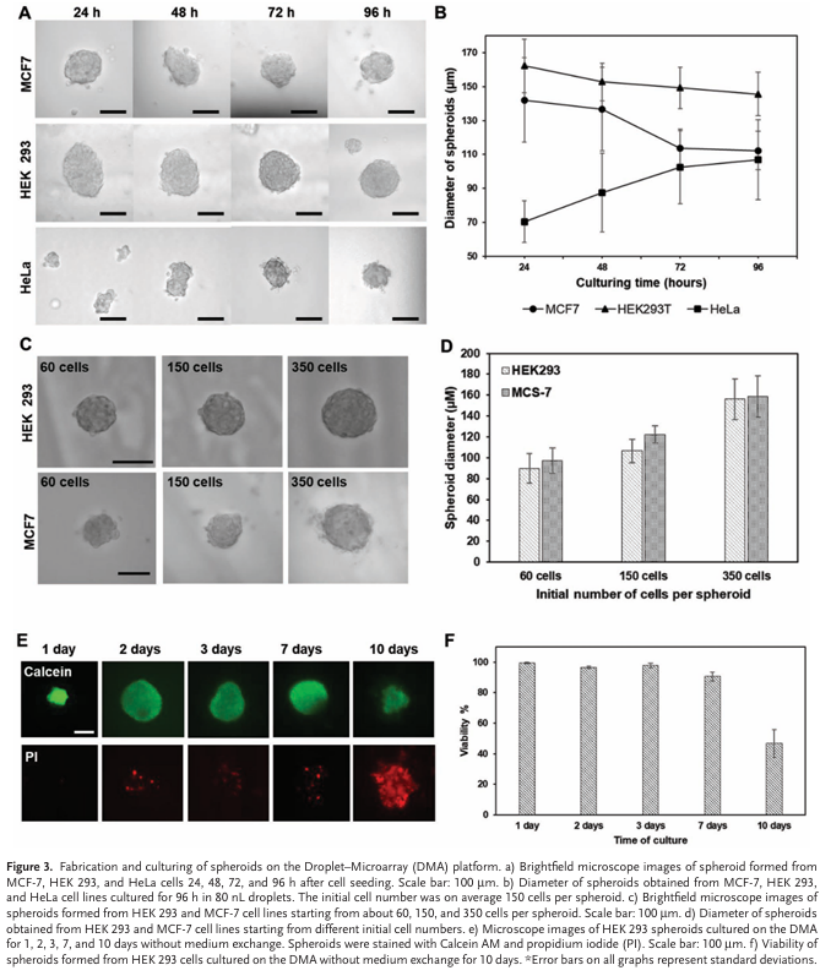
我們在不更換培養(yǎng)基的情況下對球體的生長和活力進(jìn)行了為期數(shù)天的監(jiān)測(圖 3A、B、E、F)。在培養(yǎng) 24 至 96 小時期間,HeLa 球體的直徑從 70 ± 10 微米增加到 100 ± 15 微米,而 HEK 293 球體的直徑則從 170 ± 10 微米減小到 140 ± 10 微米,MCF-7 球體的直徑則從 140 ± 20 微米減小到 110 ± 20 微米(圖 3A、B)。對于 HEK293 和 MCF-7 細(xì)胞系而言,細(xì)胞在培養(yǎng)初期就在液滴中心形成了較大的細(xì)胞團(tuán)塊,隨后在球體形成過程中細(xì)胞會逐漸緊密排列。這種在培養(yǎng)的前 2-3 天內(nèi)球體緊縮的過程已在之前得到證實。
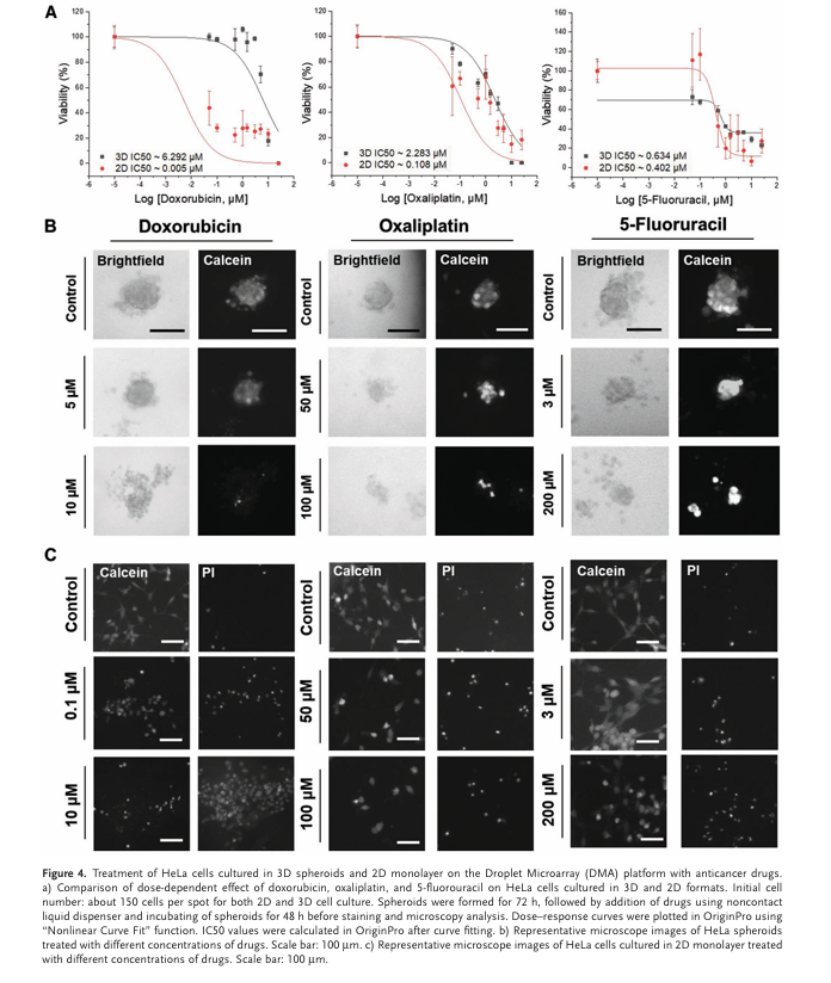
接下來,我們對由HeLa細(xì)胞形成的球體進(jìn)行了三種不同抗癌藥物(多柔比星、奧沙利鉑和 5-氟尿嘧啶)的處理,并比較了HeLa球體和在二維單層培養(yǎng)中生長的HeLa細(xì)胞的劑量反應(yīng)情況(圖 4)。使用液體分配器將HeLa細(xì)胞以每 100 納升滴液 150 個細(xì)胞的量接種,并在懸滴中培養(yǎng) 48 小時使球體形成。之后,用50 納升藥物處理球體并將液滴陣列培養(yǎng) 72 小時。對于2D細(xì)胞培養(yǎng),我們將HeLa細(xì)胞用液體分配器接種到 DMA 玻片上,并正置培養(yǎng) 5 小時以使細(xì)胞附著在表面,然相同的化合物處理,再培養(yǎng) 72 小時。最后,我們用鈣黃綠素和碘化丙啶(PI)對細(xì)胞進(jìn)行染色,分別用于可視化活細(xì)胞和死細(xì)胞。以3D和2D形式培養(yǎng)的細(xì)胞,圖 4 中顯示了劑量反應(yīng)曲線,表明這三種化合物對HeLa細(xì)胞的活力都有明顯的劑量依賴性影響。(圖 4)。3D培養(yǎng)的細(xì)胞比2D單層培養(yǎng)中的細(xì)胞更具耐藥性(圖 4),各地此前已有多次報道指出,與相同類型的單層培養(yǎng)細(xì)胞相比,腫瘤球體對抗癌化合物的抵抗力更強(qiáng)。
該研究在某些應(yīng)用中具有諸多優(yōu)勢,尤其適用于在納升滴體中對單個分離的球體進(jìn)行快速和高通量篩選,便于批量制造腫瘤球體。例如,將每個滴滴的體積縮小至 100 納升,可使化合物、試劑和細(xì)胞的使用量相比微孔板節(jié)省高達(dá) 99%。這種成本的顯著降低可能會為在藥物開發(fā)的早期階段進(jìn)行主要的超高通量篩選提供可能性,因為在這一階段會測試數(shù)百萬種化合物進(jìn)行表型篩選。每個球體只需使用 150 個細(xì)胞,這對于處理罕見且難以擴(kuò)增的細(xì)胞(如原代患者來源的腫瘤細(xì)胞)來說尤為重要。研究中使用的球體大小在 50 至 1000 微米之間不等。
研究表明,即使是直徑小于 100 微米的非常小的球體,在培養(yǎng) 2 天后也會出現(xiàn)氧梯度,并且會發(fā)展出缺氧狀態(tài)以及缺氧反應(yīng)元件(HRE)的激活現(xiàn)象,這證實了它們與體內(nèi)腫瘤在生理上的相似性。微滴陣列平臺具有靈活性,能夠通過改變初始細(xì)胞數(shù)量和親水性斑點的大小來培養(yǎng)不同大小的球體。研究表明,不同大小的球體對藥物治療的反應(yīng)可能不同,因此,應(yīng)根據(jù)應(yīng)用選擇合適的球體大小。在本研究中,我們的目標(biāo)是展示低起始細(xì)胞數(shù)量形成和篩選球體。這使得該系統(tǒng)在藥物敏感性和耐藥性測試方面具有吸引力。DMA 平臺特別適合形成具有統(tǒng)一球體大小的單個球體微陣列,這與包括 ULA 板在內(nèi)的許多其他方法不同,因為在 ULA 板中,每個孔中形成的球體的數(shù)量和大小是無法確定的。另一個優(yōu)點是可以直接在 DMA 蓋片上對球體進(jìn)行顯微鏡觀察,而無需將其轉(zhuǎn)移到微孔板中。由于小液滴的尺寸,球體的定位是固定的,這也簡化了顯微鏡觀察和圖像處理。最后,形成的均勻的細(xì)胞球體可以方便地收集到一個容器中,以供進(jìn)一步實驗使用,這對于從體外測試到再生醫(yī)學(xué)等各種應(yīng)用都非常重要。因此,本文所建立的單球體微陣列可以用于基礎(chǔ)研究、藥物發(fā)現(xiàn)以及精準(zhǔn)醫(yī)學(xué)的篩選工作流程中。




