目前,電驅(qū)動的DNA納米桿相關(guān)技術(shù),被用于檢測流感病毒,比如Influenza A/Aichi/2/1968,與其受體蛋白/肽PeB的相互作用。該受體蛋白能夠與病毒顆粒表面的血球凝集素蛋白特異性的結(jié)合。
該技術(shù)被稱為switchSENCE,其原理是將DNA鏈錨定在生物芯片的表面,并將受體肽PeB與DNA鏈進(jìn)行耦合,以實(shí)現(xiàn)將受體肽固定在芯片表面的目的。同時(shí),其中錨定在芯片表面的單鏈DNA攜帶熒光基團(tuán),而與其互補(bǔ)的DNA鏈則根據(jù)研究的需要,可以設(shè)計(jì)攜帶多價(jià)肽等受體分子。形成的雙鏈DNA納米桿,在芯片電極提供的負(fù)電壓條件下,可以保持直立的靜止?fàn)顟B(tài)。信號的檢測基于互作事件發(fā)生后,對熒光基團(tuán)周圍環(huán)境的改變,導(dǎo)致了熒光信號改變的發(fā)生。本研究中,病毒顆粒與肽的相互作用信號的產(chǎn)生說明病毒可以直接做為配體,特異性與固定在芯片表面的受體肽結(jié)合,且在較長的時(shí)間范圍內(nèi),病毒能夠保持正常活性,處于穩(wěn)定的結(jié)合狀態(tài)。此外,通過該技術(shù),可以比較不同的病毒亞型與同一受體肽的結(jié)合性能。總的來說,本研究證實(shí)switchSENCE技術(shù)可以利用病毒本身做為研究材料,在病毒顆粒原生態(tài)的環(huán)境下檢測受體與病毒表面配體的互作性能。
流行性病毒的爆發(fā),給人類的生命健康帶來極大的威脅,比如嚴(yán)重急性呼吸綜合征冠狀病毒(SARS-Cov-2)的發(fā)生及流行。帶來類似嚴(yán)重后果的還有在1918年爆發(fā)的A型流感病毒Spanish flu, 導(dǎo)致了全世界數(shù)百萬人口的死亡。A型流感病毒屬于正黏病毒科,其具有脂質(zhì)雙層膜結(jié)構(gòu),膜的表面表達(dá)三種膜蛋白:血球凝集素蛋白(HA),神經(jīng)氨酸苷酶(NA)和M2質(zhì)子通道蛋白。神經(jīng)氨酸苷酶可以促進(jìn)病毒顆粒從被感染的細(xì)胞釋放,并裂解糖苷酶鍵;HA可以在病毒與細(xì)胞融合之前,與細(xì)胞表面含有唾液酸(SA)的細(xì)胞受體結(jié)合。HA為同源三聚體結(jié)構(gòu),在其蛋白的球形頭部結(jié)構(gòu)域攜帶三個(gè)SA結(jié)合位點(diǎn)。單價(jià)肽與病毒的結(jié)合的親和性在mM級,但HA在病毒表面廣泛表達(dá),可與多個(gè)SA分子發(fā)生互作,表現(xiàn)出更高的結(jié)合性能,我們也將其稱為avidity。對病毒與其受體結(jié)合的affinity與avidity的研究,將可以幫助我們更有效的理解病毒內(nèi)化和感染的過程。由于其復(fù)雜的結(jié)合形式,需要新的技術(shù)手段對其進(jìn)行檢測分析。例如,表面等離子共振技術(shù)(SPR),核磁共振技術(shù),或者電測量等。
本研究中,我們利用switchSENCE技術(shù),對HA和其受體肽的結(jié)合動力學(xué)進(jìn)行了檢測。該技術(shù)是利用電子驅(qū)動的DNA納米桿實(shí)現(xiàn)。該DNA納米桿通過化學(xué)作用,與生物芯片進(jìn)行結(jié)合。該技術(shù)已經(jīng)廣泛用于蛋白-蛋白,蛋白-核酸適配體以及蛋白-DNA等分子之間的互作分析。而本研究是將該技術(shù)第一次用于病毒-肽的互作檢測。
switchSENCE技術(shù),不僅可以檢測分子互作之間的親和性(KD),同時(shí)可以實(shí)時(shí)檢測結(jié)合常數(shù)(Kon)和解離常數(shù)(Koff)。在藥物發(fā)現(xiàn)研究領(lǐng)域,這些分子互作參數(shù),對于潛在藥物性能的評估至關(guān)重要。分子互作的親和性,可以通過傳統(tǒng)的MST,ITC等技術(shù)進(jìn)行檢測,但是它們無法測量實(shí)時(shí)的結(jié)合和解離常數(shù),并且需要進(jìn)行熒光標(biāo)記,而switchSENCE技術(shù)可以在不標(biāo)記互作分子的情況下,檢測其相互作用動力學(xué)參數(shù)。與其相似的傳統(tǒng)技術(shù)有表面等離子共振技術(shù)(SPR),兩者在測量分子互作方面具有非常多的相似性和優(yōu)點(diǎn),比如:(1)不僅可以測量親和性,同時(shí)可以實(shí)時(shí)檢測動力學(xué)參數(shù);(2)都不需要進(jìn)行標(biāo)記;(3)較低的樣本消耗量;(4)數(shù)據(jù)檢測的較高靈敏度;兩種技術(shù)也有相似的不足之處,比如:(1)都需要將其中一個(gè)分子進(jìn)行固定,固定本身可能會影響分子互作性能的檢測;(2)微流控下的物質(zhì)運(yùn)動的限制;(3)非特異性結(jié)合發(fā)生的可能性。不論是SPR還是switchSENCE技術(shù),對數(shù)據(jù)的解讀都非常重要,需要研究人員的經(jīng)驗(yàn)和對儀器的深入了解,以實(shí)現(xiàn)對結(jié)果進(jìn)行科學(xué)合理的評估。
和SPR相比,switchSENCE技術(shù)具有相應(yīng)的優(yōu)勢,其中之一是可以控制受體在其表面結(jié)合的密度,以減少分子的聚集,并可以按照不同比例分布兩種不同的分子。此外,switchSENCE技術(shù)由于利用了DNA互補(bǔ)雜交原理,因此可以應(yīng)用于多種類型的分子互作場景;尤其當(dāng)待檢測的受體分子是DNA為基礎(chǔ)的結(jié)構(gòu),比如DNA-肽納米結(jié)構(gòu),更具有操作上的優(yōu)勢。除此之外,switchSENCE技術(shù)還能夠用于測量蛋白構(gòu)象變化以及流體動力學(xué)半徑測量,這些是SPR無法實(shí)現(xiàn)的功能。
PeB受體肽起源于單克隆抗體HC19免疫球蛋白可變區(qū)域的互補(bǔ)決定區(qū),已經(jīng)報(bào)道,其對HA2, NA3具有中和效應(yīng)。已經(jīng)證實(shí),它能夠與A型流感病毒株Aichi H3N2的HA蛋白結(jié)合,其親和性在uM級。雖然該親和性相比單價(jià)分子間親和性已大大提高,對于治療型抗體的效率來說,仍舊需要進(jìn)一步優(yōu)化和提高。
為了實(shí)現(xiàn)進(jìn)一步優(yōu)化的目的,許多改進(jìn)的方法嘗試多價(jià)互作的形式,以增強(qiáng)小分子配體與生物受體復(fù)合物的靶向效率。對于流感病毒的HA受體,其唾液酸配體的結(jié)合位點(diǎn)為有序排列的三聚體復(fù)合物,兩個(gè)鄰近位點(diǎn)之間的距離大約為4.2nm。在一些實(shí)驗(yàn)設(shè)計(jì)中,以DNA或其它核酸為基礎(chǔ)的納米桿,已經(jīng)做為一種呈遞HA結(jié)合配體的骨架,應(yīng)用于研究中。由于該骨架操作的靈活性,可以呈遞單價(jià),二價(jià)或三價(jià)配體,因此提高了分子之間的結(jié)合性能;該設(shè)計(jì)的第二個(gè)優(yōu)勢,體現(xiàn)在遵循沃森-克里克的堿基互補(bǔ)配對原則的DNA骨架設(shè)計(jì),使得多種類型的分析檢測更加的直觀化。通過延長非配對的單鏈序列,使其可以做為簡單的模塊,與互補(bǔ)配對鏈共同錨定在分析檢測表面。例如,本研究第一次報(bào)道了,利用switchSENCE技術(shù)對病毒與錨定在芯片表面的DNA-肽的互作動力學(xué)進(jìn)行檢測。
互作分析通過以switchSENCE技術(shù)為基礎(chǔ)的DRX2(Dynamic Biosensors GmbH, Germany)儀器實(shí)現(xiàn)。使用的芯片為MPC-48-1-R1-S 或 MPC2-48-2-G1R1-S(Dynamic Biosensors GmbH)。每個(gè)微流控芯片由四個(gè)獨(dú)立的液流通道組成,詳情見Figure 1a。

Figure 1: 生物芯片結(jié)構(gòu)及DNA納米桿結(jié)構(gòu)示意圖
每一個(gè)通道寬1mm, 高60um, 包含六個(gè)金屬電極,長度為3.34mm, 每個(gè)電極直徑為120um, 其與電源相連。每一個(gè)電極都與DNA納米桿相連接。單鏈DNA納米桿(NL-B48,序列請見Table 1)通過5’端與芯片表面共價(jià)結(jié)合,在序列3’端攜帶有用于信號檢測的熒光基團(tuán)。互補(bǔ)配對的DNA鏈(cNL-B48,序列請見Table 1),可以與待檢測的目標(biāo)分子進(jìn)行交聯(lián)。在本研究中,受體肽(SA)與互補(bǔ)配對的DNA鏈進(jìn)行交聯(lián)。通過DNA分子雜交,使得互補(bǔ)配對鏈DNA-肽與芯片表面的DNA鏈進(jìn)行結(jié)合,形成雙鏈DNA。該雙鏈DNA可以用于后續(xù)的電驅(qū)動的互作分子檢測。其結(jié)構(gòu)請參見Figure 1。由于電源可以交替產(chǎn)生正/負(fù)電壓(AC),因此能夠使得帶有負(fù)電荷的雙鏈DNA在芯片表面進(jìn)行擺動,被稱為“dynamic mode”;電源也可以是保持不變的負(fù)電壓(DC),使得DNA雙鏈保持直立狀態(tài),被稱為“static mode”。對于動力學(xué)模式,AC電壓的范圍是-0.3V到0.5V,變化頻率為10kHz. 在動力學(xué)模式下進(jìn)行測量時(shí),當(dāng)DNA雙鏈接近金屬電極時(shí),由于發(fā)生能量轉(zhuǎn)移,熒光信號發(fā)生淬滅,當(dāng)其離開芯片表面時(shí),熒光強(qiáng)度增強(qiáng),進(jìn)而產(chǎn)生周期性的熒光信號的改變。改變過程中發(fā)生的熒光光子數(shù),通過實(shí)時(shí)的單光子計(jì)數(shù)技術(shù)(e-TCSPC)進(jìn)行檢測。在結(jié)合事件發(fā)生后,由于整體納米桿的流體動力學(xué)摩擦系數(shù)的增加,造成了DNA納米桿在該流體系統(tǒng)中運(yùn)動速率的減慢,速率的變化可以通過實(shí)時(shí)的熒光變化進(jìn)行檢測。在靜止模式下,電壓可以保持在固定數(shù)值,本研究中為-0.1V,DNA保持在直立靜止?fàn)顟B(tài)。該狀態(tài)下,由于結(jié)合事件的發(fā)生,導(dǎo)致熒光基團(tuán)周圍的生化,物理等環(huán)境的改變,熒光基團(tuán)的信號發(fā)生改變,這種改變不受所結(jié)合的分子大小的影響,而是受結(jié)合位點(diǎn)周圍化學(xué)環(huán)境的影響,因此主要依賴于互作的類型。

Table 1 DNA納米桿構(gòu)成序列
DNA按照Table 1中的序列進(jìn)行合成。cNL-B48和NL-W48-B48-G1購于Dynamic Biosensors GmbH,寡核苷酸p-cNL-B48, n, n*o, 和 o*p* (見Table 1) 購于Biomers.net. p-cNL-B48寡核苷酸鏈可以部分的與固定在芯片表面的NLB-48核酸鏈互補(bǔ)。攜帶有氨基基團(tuán)的寡核苷酸鏈(p-cNL-B48, n*o, o*p*)與PeB肽進(jìn)行交聯(lián)并進(jìn)行純化;隨后,攜帶PeB肽的寡核苷酸鏈折疊成四臂結(jié)構(gòu),請見Figure 2。在進(jìn)行動力學(xué)檢測之前,肽與寡核苷酸的耦合效率可以通過非變性聚丙烯酰胺凝膠電泳進(jìn)行質(zhì)量評估。該遞呈肽的DNA結(jié)構(gòu),在未與肽結(jié)合時(shí)分子量為43kDa,與三肽結(jié)合后的分子量為49kDa.
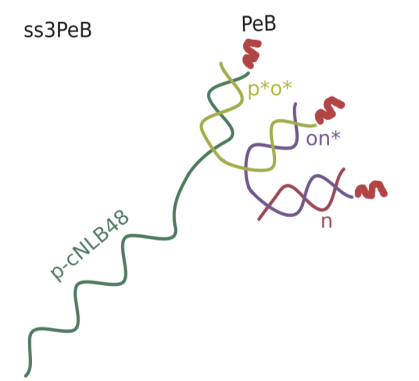
Figure 2 寡核苷酸-三肽偶合結(jié)構(gòu)
分子互作檢測通過DRX2儀器(Dynamic Biosensors GmbH, Martinsried, Germany)進(jìn)行。在本測量中,使用的生物芯片序列號為MPC-48-1-R1-S 或MPC2-48-2-G1R1-S(Dynamic Biosensors GmbH)。測量實(shí)驗(yàn)流程通過switchBUILD軟件實(shí)現(xiàn),并通過switchCONTROL軟件逐步實(shí)行(軟件由Dynamic Biosensors GmbH提供)。芯片上每一個(gè)微流控通道在正式檢測前,需要使用含有硫醇基的鈍化溶液進(jìn)行處理,然后進(jìn)行芯片質(zhì)量檢測,以保證芯片在良好的狀態(tài)下檢測到最大強(qiáng)度的熒光信號。DNA鏈以500nM的濃度與芯片進(jìn)行雜交,雜交時(shí)間為320s,該互作動力學(xué)檢測在靜止模式下進(jìn)行。底物的分析濃度范圍為10-40ug/ml。對于結(jié)合過程,底物上樣體積為50ul,流速為1ul/min,結(jié)合時(shí)間為50min; 對于解離過程,流速為3ul/min,解離時(shí)間為13.3分鐘。
在三明治模式的動力學(xué)檢測中,使用的是NL-W48-B48-G1寡核苷酸鏈,其部分與cNL-B48互補(bǔ)。該寡核苷酸鏈攜帶有綠色熒光基團(tuán)。在檢測之前,DNA鏈(NL-W48-B48-G1 和DNA 納米結(jié)構(gòu)ss1/2/3PeB)進(jìn)行雜交,使得DNA納米結(jié)構(gòu)標(biāo)記上綠色熒光,用于后續(xù)檢測。兩條互補(bǔ)寡核苷酸鏈以1:1的比例混合,避光室溫孵育1小時(shí)。三明治檢測模式是以ss2PeB做為配體,將病毒X31進(jìn)行捕獲,然后以肽-DNA 結(jié)構(gòu)ss1/2/3PeB-NL-W48-B48-G1做為底物進(jìn)行上樣分析其與病毒結(jié)合的動力學(xué)。該測量在swithcSENCE靜止模式下進(jìn)行。
相互作用檢測的基礎(chǔ)為與芯片耦合的攜帶熒光基團(tuán)的DNA寡核苷酸鏈(NL-B48)以及與其互補(bǔ)配對的攜帶有受體肽的寡核苷酸鏈。病毒顆粒在該檢測中,做為底物進(jìn)行上樣分析。DNA之間雜交形成納米結(jié)構(gòu)是在動力學(xué)模式(dynamic mode)下進(jìn)行(請見Figure 3),病毒顆粒的結(jié)合是在靜止模式下進(jìn)行(static mode)。熒光基團(tuán)信號的變化,表征結(jié)合事件的發(fā)生。DNA鏈雜交后,檢測將轉(zhuǎn)為靜止模式,DNA-肽結(jié)構(gòu)處于直立靜止?fàn)顟B(tài)。本檢測中,互補(bǔ)配對的第二條DNA寡核苷酸鏈具有四個(gè)核苷酸臂,其中之一部分與固定在芯片上的NL-B48單核苷酸鏈進(jìn)行互補(bǔ),其余三條臂分別攜帶一個(gè)肽分子PeB。在具體實(shí)驗(yàn)中,可靈活設(shè)計(jì)攜帶有單個(gè),二個(gè),三個(gè)或不攜帶肽分子的DNA結(jié)構(gòu)。Figure 3b表示的是cNLB48以及ss3PeB和固定在芯片上的NLB-48雜交的示意圖。雜交的過程,提供的是交替變換的電壓,在互補(bǔ)配對鏈結(jié)合之前,單鏈DNA的運(yùn)動是比較微弱的,可能由于單鏈結(jié)構(gòu)的靈活性,使得熒光基團(tuán)與芯片表面的距離比較接近,熒光信號變化幅度較低。一旦與互補(bǔ)鏈配對,請見Figure 3, 雙鏈DNA的移動幅度大大增加,熒光信號變化的幅度隨之提升。從Figure 3可以得知,相比于未攜帶肽分子的互補(bǔ)配對鏈, ss3PeB與NL-B48雜交的效率更高,這可能是由于大分子擴(kuò)散速率慢,且DNA雙鏈更長,攜帶更多的負(fù)電荷。
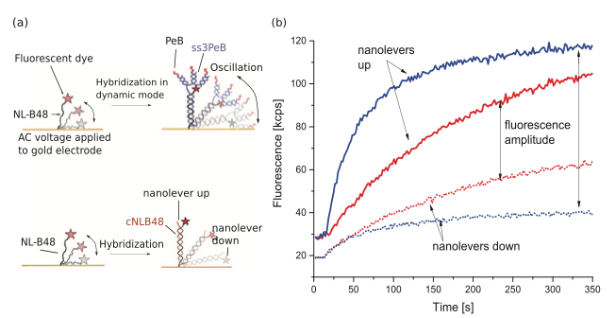
Figure 3 芯片雜交信號檢測
芯片雜交完成后,病毒顆粒做為底物進(jìn)行上樣,與肽分子進(jìn)行結(jié)合。請見Figure 4。數(shù)據(jù)以ss2PeB與病毒的結(jié)合進(jìn)行展示。在結(jié)合過程中,保持1ul/min的低液流速率,以保證反應(yīng)不受快速擴(kuò)散的影響。因?yàn)镈NA納米桿的長度大約為20nm,圓形病毒顆粒的平均直徑大約為120nm,桿狀病毒顆粒的長度約為300nm。因此單個(gè)病毒可能與一個(gè)以上的DNA納米桿單位進(jìn)行結(jié)合。

Figure 4 病毒顆粒與ss2PeB結(jié)合示意圖
Figure 5展示了不同濃度的X31病毒顆粒和ss2PeB結(jié)合的動力學(xué)。X31病毒顆粒經(jīng)液流注入系統(tǒng)后,即可觀察到濃度依賴的熒光信號減少的發(fā)生。在每一次測量后,芯片都需要再生,然后重新進(jìn)行DNA鏈的雜交。經(jīng)實(shí)驗(yàn)觀察發(fā)現(xiàn),在極限的750s解離時(shí)間內(nèi),病毒顆粒仍舊穩(wěn)定的結(jié)合在DNA納米桿結(jié)構(gòu)上。從已有的報(bào)道可知,病毒蛋白與其受體結(jié)合的親和性在uM級,這與該實(shí)驗(yàn)中觀測到的解離結(jié)果不符。這可能是由于在該研究中,病毒顆粒與受體的結(jié)合是多價(jià)模式,導(dǎo)致了結(jié)合的avidity效應(yīng)的發(fā)生,結(jié)合更加的穩(wěn)定。因此,這種方法使得對真實(shí)的親和性的檢測受到限制。做為陰性對照,ss0PeB(DNA鏈未與肽分子偶聯(lián))用于檢測病毒顆粒的非特異性結(jié)合。結(jié)果表明,病毒顆粒與肽的結(jié)合是特異性的。

Figure 5 X31病毒顆粒與ss2PeB結(jié)合動力學(xué)
該實(shí)驗(yàn)設(shè)計(jì)是將病毒顆粒做為生物材料,固定在芯片表面,目的是為了檢測到受體肽與其結(jié)合的解離常數(shù)及親和性。在本研究中,ss2PeB與芯片進(jìn)行雜交,形成雙鏈DNA納米桿,經(jīng)由DNA鏈被標(biāo)記成紅色熒光;隨后,X31病毒顆粒被ss2PeB捕獲。在上述實(shí)驗(yàn)中發(fā)現(xiàn),在整個(gè)過程中,病毒顆粒與肽的結(jié)合非常牢固,無解離的發(fā)生,因此可將該病毒顆粒做為固定的配體,進(jìn)行后續(xù)的二次動力學(xué)結(jié)合檢測。可將標(biāo)記綠色熒光基團(tuán)的肽-DNA鏈做為分析底物,與固定結(jié)合的病毒進(jìn)行結(jié)合。
Figure 6展示了該實(shí)驗(yàn)設(shè)計(jì)的原理圖。ss2PeB-G1與X31的結(jié)合,導(dǎo)致了綠色熒光通道信號的逐步增強(qiáng)。對于結(jié)合的起始點(diǎn),該模式中也有了明顯的信號改變。總的來說,無論是結(jié)合還是解離,該模式下的熒光信號改變都非常明顯,能夠讓研究人員更加準(zhǔn)確的判斷結(jié)合的起始和解離的過程。通過該三明治模式,可以對肽與病毒結(jié)合的解離動力學(xué)進(jìn)行研究。在本研究中,經(jīng)測量,兩者的結(jié)合常數(shù)為 kon = (1.8 ± 0.8) × 10 5 M ?1 s?1 ,解離常數(shù)為 koff = (2.3 ± 0.2) × 10 ?3 s?1,親和性為KD = (12 ± 7) nM。未捕獲病毒的DNA納米桿做為對照,用以排除非特異性結(jié)合。除了ss2PeB,單價(jià)肽ss1PeB-G1和三價(jià)肽ss3PeB-G1也進(jìn)行了相應(yīng)的檢測,三種復(fù)合物得到了較為相似的結(jié)合和解離動力學(xué)常數(shù)。ss1PeB-G1, KD = (12 ± 9) nM ,ss3PeB-G1, KD=(8 ± 7) nM.

Figure 6 三明治模式檢測病毒與肽結(jié)合的動力學(xué)
本研究證實(shí)了DNA納米結(jié)構(gòu)可以用于病毒-肽的互作動力學(xué)分析。利用switchSENCE技術(shù),將PeB與DNA單鏈進(jìn)行耦合,并與A型流感病毒X31進(jìn)行結(jié)合,該結(jié)合信號隨病毒濃度的變化而變化。但由于兩者結(jié)合中的多價(jià)效應(yīng)存在,無法通過該模式對解離動力學(xué)進(jìn)行檢測。在三明治設(shè)計(jì)模型中,我們可以實(shí)現(xiàn)同時(shí)對結(jié)合和解離動力學(xué)進(jìn)行分析,進(jìn)而得到兩者互作的親和性。在這種模式下,兩者之間的多價(jià)效應(yīng)對動力學(xué)檢測的影響較小。后續(xù)對于該技術(shù)更深入的探索研究,可以對DNA納米骨架進(jìn)行優(yōu)化(比如單臂的長度,中心結(jié)點(diǎn)的靈活度等),以最大程度的減小單價(jià)遞呈模塊對結(jié)合動力學(xué)的影響。目前,由于測量誤差太大還不能夠區(qū)分單價(jià)結(jié)合的親和性常數(shù),需要更長的解離時(shí)間以達(dá)到檢測的目的。總的來說,進(jìn)行病毒-肽之間的互作動力學(xué)分析,在傳統(tǒng)的SPR技術(shù)中遇到了一定的阻礙。由于病毒顆粒結(jié)構(gòu)和蛋白表達(dá)的豐度,需要考慮受體的密度,物質(zhì)的流動速率以及樣本制備等方面。在switchSENCE技術(shù)中,受體的密度可以通過單鏈DNA納米桿的數(shù)量進(jìn)行控制。實(shí)驗(yàn)后芯片再生的過程,也會影響到受體的密度,減少了芯片上高質(zhì)量納米桿的數(shù)量,這是在實(shí)驗(yàn)的重復(fù)性驗(yàn)證方面需要進(jìn)行考慮的問題;對于物質(zhì)轉(zhuǎn)運(yùn)的限制,可以通過減少芯片上受體的數(shù)量以及增加流速解決。然而,芯片上受體數(shù)量的減少的同時(shí),還需要考慮儀器整體的信噪比。對于多價(jià)結(jié)合的動力學(xué)曲線,單指數(shù)模型無法準(zhǔn)確的擬合,需要更多的擬合模型應(yīng)對復(fù)雜的互作動力學(xué)結(jié)果。總的來說,switchSENCE技術(shù)可以廣泛的應(yīng)用到肽的優(yōu)化,病毒與不同受體,包括核酸適配體,肽,抗體或者蛋白等分子結(jié)合的定量和定性分析,并且該技術(shù)可以更方便的用于單價(jià)和多價(jià)結(jié)合動力學(xué)分析。




