在組織工程和再生醫學領域,人工多細胞系統正變得日益重要。然而,體外重建復雜的組織結構充滿挑戰,急需能夠可控且高通量制造復雜多細胞結構的方法。該文介紹一種創新的3D細胞培養方法——基于可編程液滴融合技術的多球狀細胞結構組裝(proMAD方法)。這一方法不僅能夠精確控制細胞組成和空間分布,還能在迷你化、高通量的格式下重建模擬天然組織的復雜性,可應用于細胞信號、腫瘤侵襲、胚胎發生和神經發育等多種生物過程的研究。
I.DOT非接觸式移液器:
proMAD方法的技術核心及優勢

proMAD方法無需支架,可以以高通量和小型化的方式自動形成球形組件陣列,以解決細胞-細胞通信中使用的細胞機制的復雜性。該方法的核心在于I.DOT非接觸式移液器,它能夠在納升至微升的范圍內,非接觸式地將液體從源頭轉移到目標板。這意味著極低的死體積(<1 μL)和零交叉污染風險,為細胞培養提供了前所未有的精確度和安全性。
與此同時,I.DOT搭載的DropDetection系統,能夠對每個液滴進行計數和檢測,提供液體轉移性能和總體積的即時反饋。這不僅確保了實驗的可重復性和可靠性,還極大地提高了實驗效率。
利用該文作者已開發的液滴微陣列(DMA)平臺[1-3],它可以制造納米升液滴微陣列,其中液滴的形狀、大小和密度取決于被超疏水屏障包圍的親水性圖案的設計。DMA平臺可以在數百個單獨的納升液滴中培養和高通量篩選各種細胞類型,這些液滴作為獨立的小型化棲息地[4]。
在DMA平臺上使用懸滴法制備單細胞球體,使用了由14 × 14個親水點(每個1 mm × 1 mm)組成的DMA,點之間的距離為500 μm(圖1)。以HepG2細胞為例,將細胞懸液以200 nL的液滴形式通過I.DOT非接觸式移液器分配在DMA上,每個液滴含有的細胞數量可控制球體直徑(30-150 μm)。然后將DMA倒置,使細胞在液滴-空氣界面因重力驅動聚集,培養2天后形成單個球體(圖1a,1b)。采用以下打印順序:為融合4個液滴,將培養基依次添加到D2、E2、D3、E3點(圖1c中藍色點,每個點多添加900 nL DMEM);為了融合3個液滴,將培養基依次添加到A1、A2、B2點(圖1f中藍色點,每個點增加850 nL DMEM)。然后相鄰的液滴融合成一個。將載玻片倒置培養24、48、72、96 h。用Keyence軟件對球體或合并球體進行觀察和成像。
proMAD方法的基礎是將額外體積的細胞培養基分配到相鄰的單個液滴中,并控制它們在超疏水屏障上的融合(圖1)。在相鄰的每個200 nL的液滴中加入900 nL的介質(即每個點總共加入1100 nL),相鄰的液滴會自發合并成一個新的大液滴,并牢固地附著在兩個親水點上(圖1)。合并液滴后,將DMA載玻片再次倒置進行培養,使先前分離的兩個球體在液滴底部接觸,并使它們粘附融合成多球體復合物(圖1a)。同樣,通過增加多個相鄰液滴的體積來合并兩個以上的液滴(圖1c-h)。有趣的是,這導致了由多個單獨的細胞球體組成的融合球體的形成。為了融合兩種不同的細胞系,選擇了兩種不同的細胞系:HeLa RFP細胞和HEK 293T細胞。用共聚焦顯微鏡檢查合并的球體。
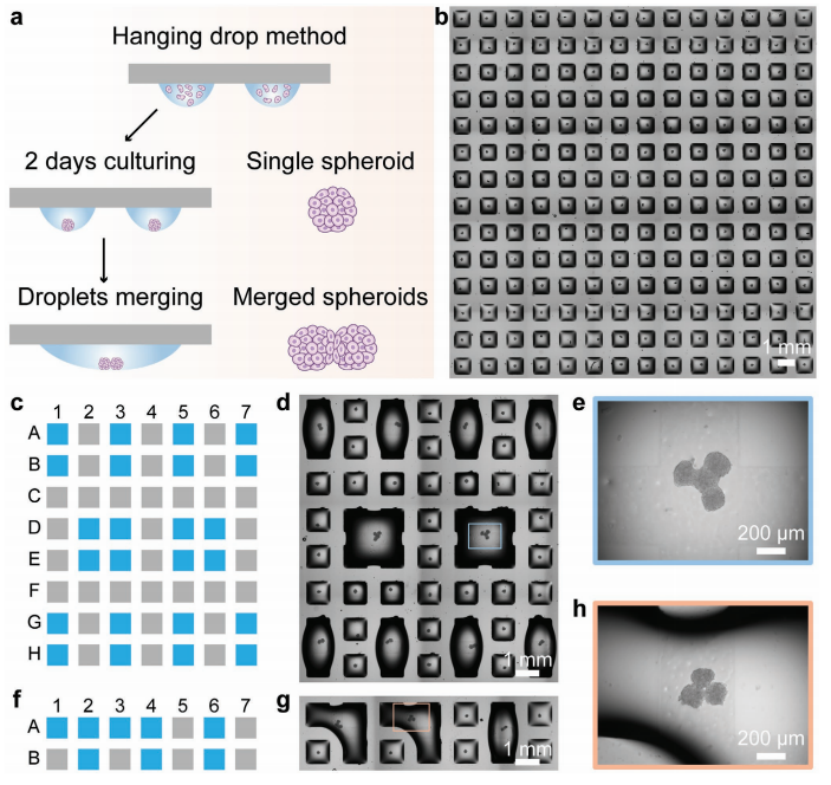
圖1. 可編程液滴融合技術(proMAD)。a)利用親水點被超疏水邊界分隔的小型化液滴微陣列(DMA)形成細胞球體陣列的示意圖。為了實現球體的可編程裝配,通過增加相鄰液滴的體積來合并液滴。b)單個HepG2球體14 × 14陣列顯微鏡圖像。c, f)多液滴在DMA上可控合并的打印方案。使用以下印刷體積:900 nL /液滴,用于融合2或4個液滴;850 nL /液滴,將3個液滴融合在一起((c)和(f)中的藍色點)。d, g)含有2、3和4個合并液滴的DMA顯微鏡圖像。e, h)融合24 h后融合水滴中的4個球體和3個球體圖像
1. 球體特征分析:使用ImageJ軟件測量和計算球體的圓形度、縱橫比、圓度和密實度等參數[5];
2. 融合過程分析:通過ImageJ軟件的角度工具測量兩個融合球體在不同融合時間點的夾角,用長度測量工具測量兩個球體之間融合區域(“頸部”)的長度[5];
3. 細胞活力檢測:融合后24 h收集雙球體,用 PBS 洗滌后,用 Calcein- AM和碘化丙啶染色15 min(37°C),然后通過熒光顯微鏡成像檢測細胞活力[5];
4. 免疫染色:收集并洗滌球體后,用 4% 多聚甲醛固定,0.5% Triton X - 100 透化,1% BSA 封閉,依次加入抗 - E - 鈣粘蛋白抗體和 Alexa Fluor 488 標記的二抗,最后用 DAPI 染色,通過共聚焦顯微鏡成像[5];
5. 掃描電鏡固定:融合后 24 h 收集球體,用 PBS 洗滌,依次用 2.5% 戊二醛溶液固定、不同濃度乙醇和水脫水、50% 和 100% HMDS 處理,然后轉移到干凈玻片上干燥,通過掃描電子顯微鏡成像[5]。
6. 球體間Wnt信號傳導:產生HEK 293T Wnt-3a,以及穩定的HEK 293T TOP-GFP報告細胞系按照規劃程序進行播種[6]。將產生Wnt的細胞打印在第1、3、5、7、9、11、13列,報告細胞打印在第2、4、6、8、10、12、14列。掛滴法培養2天后,每個點加入900 nL DMEM合并相鄰點。為了研究Wnt信號傳導,每24小時用熒光顯微鏡和共聚焦顯微鏡檢查合并的球體。
1、對于融合的球體,定義了 “結合數” 來描述單個球體在融合過程中與相鄰球體的作用。在這個過程中,I-DOT對前期球體的精準分配影響了后續融合的球體的各種數據。通過模擬算法和實驗結果統計量化了合并球體 “結構異構體” 的組合概率。例如,3個球體融合時有兩種可能的結構,線性組合A1A2A1和三角形結構A2A2A2,實驗概率分別為61% 和39%,模擬算法得到的概率分別為85%和15%(圖2a);
除了融合可變數量的同源球體外,還可以融合由不同細胞類型形成的球體(圖2b)。在多細胞生物中,組織由多種具有空間組織的細胞類型組成,這些細胞類型協同工作以執行特定功能。圖2b的結果顯示,即使在融合過程24小時后,異質球體中兩種細胞類型之間仍有明確的邊界。因此,proMAD方法可以通過合并特定數量的相鄰液滴來實現單個球體的可控組裝,從而產生多球體聚集體,以及陣列格式的異質球體架構。
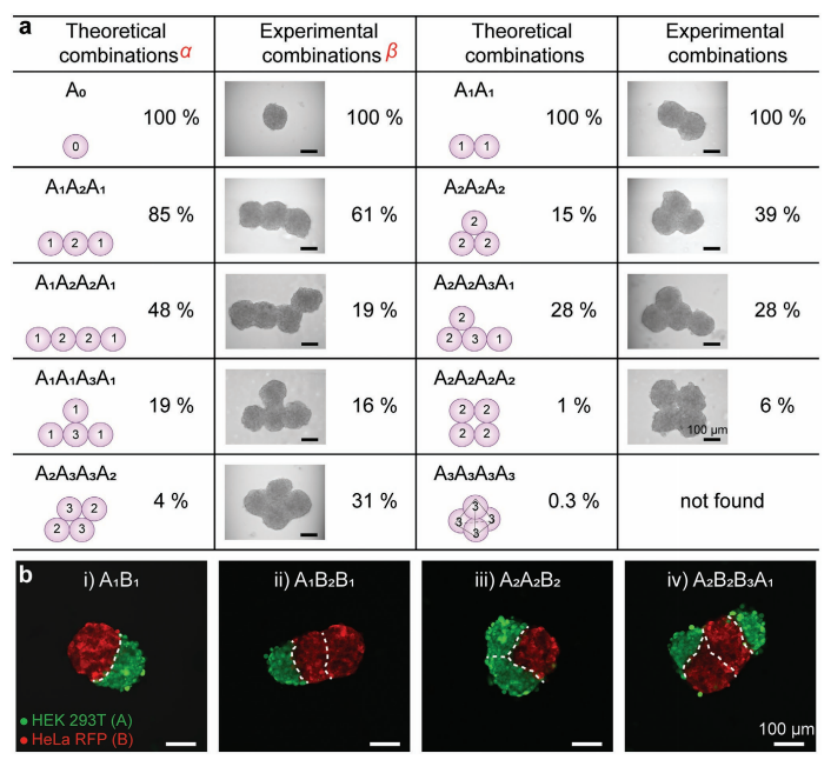
圖2. 由proMAD方法形成的多球體結構的例子。a)不同HepG2多球體的示意圖、概率和相應的例子。“結合數”對應于配合物的各個球體之間的結合位點的數量,顯示在方案上的每個球體中。α,在理論模型中,將細胞球體視為球體,并通過模擬算法給出組合概率。β,組合概率由實驗統計得出(3個球體,n = 33, 4個球體,n = 32)。b)兩種不同細胞系(表達RFP和HEK 293T的HeLa細胞用綠色熒光5-氯甲基熒光素雙乙酸酯染色)合并后24小時構建的異球結構的熒光顯微鏡圖像:A1B1,A1B2B1,A2A2B2和A2B2B3A1。
2、為了觀察球體融合的過程,我們在液滴融合后的5天內,在規定的時間點用顯微鏡監測了兩個球體融合在一個液滴中的情況(圖3a)。兩個HepG2球體首先融合成花生狀結構,水滴融合后24-96 h形成固體融合橢圓形結構(圖3a)。在觀察兩個球體融合過程中,測量了融合點的切線角度和融合區域的長度。融合2 h后,兩個原始球體的形狀仍可清晰辨認,夾角在57° ± 16°到154° ± 11°之間,融合區域長度約為40.7 ± 6.8 μm;48 h后夾角大于,96 h完全融合時夾角接近,融合區域長度逐漸增加到138 ± 10μm(圖3c),共培養48 h后,合并后96 h,兩個球體之間的夾角在110°以上,逐漸接近180°,完全融合(圖3a,b)。我們稱之為“頸部”的合并區域的長度(圖3a,橙色虛線)。
此外,作者還使用細胞-細胞相互作用模型來模擬兩個球體的融合過程(圖3d)[7]。熱圖(圖3e)顯示了融合過程中單個細胞的相對位移,表明球體中的細胞已經重新分布,形成新的橢圓形結構。在我們的實驗和模擬中,融合后96 h雙球體的總長度分別減少了約18%。
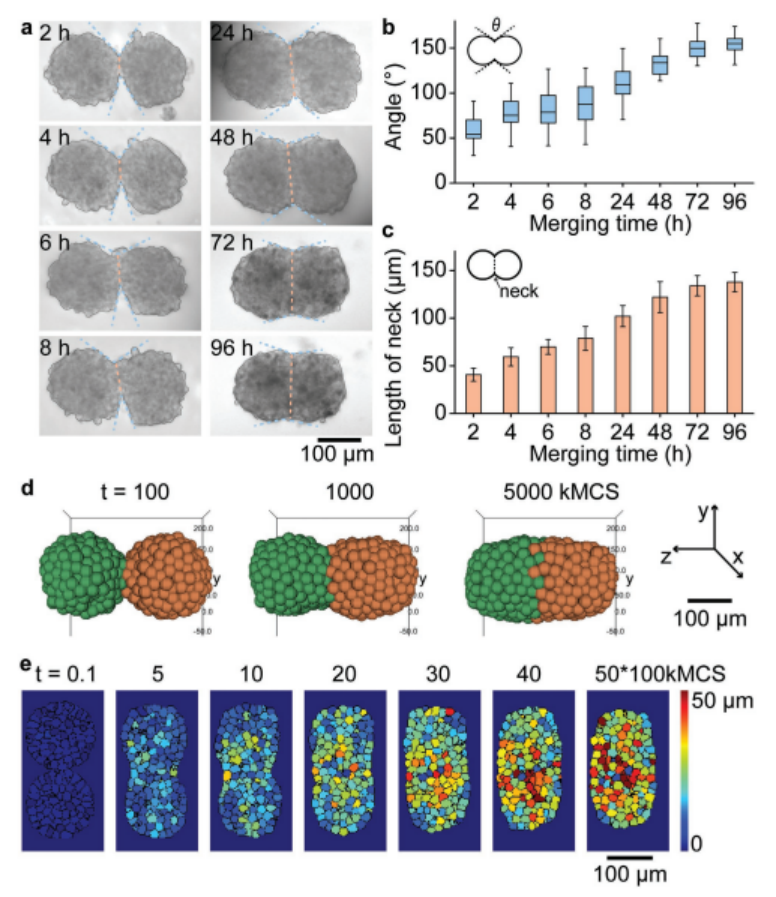
圖3. 兩胞球體融合過程的實驗與模擬研究。a)兩個HepG2球體初次接觸96小時后融合的亮場顯微鏡圖像。b)合并球體間夾角隨時間變化的曲線圖。(a)中的藍色虛線表示角度。c)顯示合并球體隨時間變化的頸部長度(橙色虛線顯示在(a)中)的圖。(b)和(c)中的誤差條表示10個不同合并球體的SD。d)兩個球體(球體直徑150μm, 400個細胞)融合過程的三維模擬。e)熱圖顯示融合過程中單個細胞的時空運動。彩色地圖表示每個細胞相對于其初始位置的位移(t = 0)。kMCS是時間尺度,代表kilo Monte Carlo sweep。
3、為觀察兩球體合并區域細胞狀況,進行了E-cadherin免疫染色和掃描電鏡成像(圖4a)。E-cadherin免疫染色用于可視化細胞粘附和連接[8],結果顯示在融合的雙球體內均勻分布,表明球體是生物融合而非物理吸附。掃描電鏡成像證實了 “花生” 形融合復合體的形成及單個球體界面細胞間的緊密相互作用(圖4b)。這些結果表明,用特定方法獲得的多球體三維結構,在球體之間具有緊密的細胞間接觸,利于研究細胞間相互作用及相關生物過程。

圖4. 兩胞球體融合過程的實驗與模擬研究。多球體結構中的細胞-細胞相互作用。a)融合24 h后兩個HepG2球體的熒光顯微鏡圖像。e -鈣粘蛋白染色(綠色熒光)顯示細胞間連接。DAPI(藍色熒光)顯示細胞核。合并:DAPI覆蓋層,E-Cadherin染色。b)融合后球體(HepG2,融合后24 h)的SEM圖像。左圖是在2000倍放大率下拍攝的。右上方圖像(藍框)在7000倍放大下顯示單個球體內細胞-細胞接觸。右下角(橙色框)在7000倍放大下顯示了雙球體的接觸“頸部”區域。
4、使用proMAD方法將產生Wnt的球體(HEK 293T, Wnt-3a)與報告球體(HEK 293T, TOP-GFP)融合(圖5a)。融合后24和48小時,通過測量TOP-GFP報告球體的熒光強度來監測Wnt信號活性(圖5b)。報告球體共培養24 h后平均熒光強度為45.3 ± 10.0,共培養48 h后平均熒光強度為58.3 ± 5.7(圖5b)。共培養48小時后,整個報告球體顯示出均勻的GFP熒光,表明在球體的所有細胞中Wnt信號被強烈激活(圖5c-i,ii)。對照實驗僅顯示較弱的GFP強度(圖5c-i,ii) [9,10],融合后24和48 h的平均熒光強度分別為3.0 ± 1.1和2.9 ± 0.9。在Wnt-3a存在下,TOP-GFP Wnt報告球體的熒光強度比對照球體增加了約15倍(24 h)和大約20倍(48 h)。
接下來,研究測試了Wnt信號在三重球體復合體中的傳播,將兩個報告球體與一個產生Wnt-3a的球體合并,然后選擇兩種不同的融合球體架構進行分析。在第一種結構中,兩個報告球體呈線性結構排列,產生Wnt的球體位于一端(圖5d)。與產生Wnt直接相鄰的報告球體被強烈激活,而位于遠端的報告球體被不那么強烈激活(圖5d,f)。在第二種組合中,兩個報告球體位于生產者球體的兩側,顯示出兩個報告球狀體在同等程度上的強烈激活(圖5e,g)
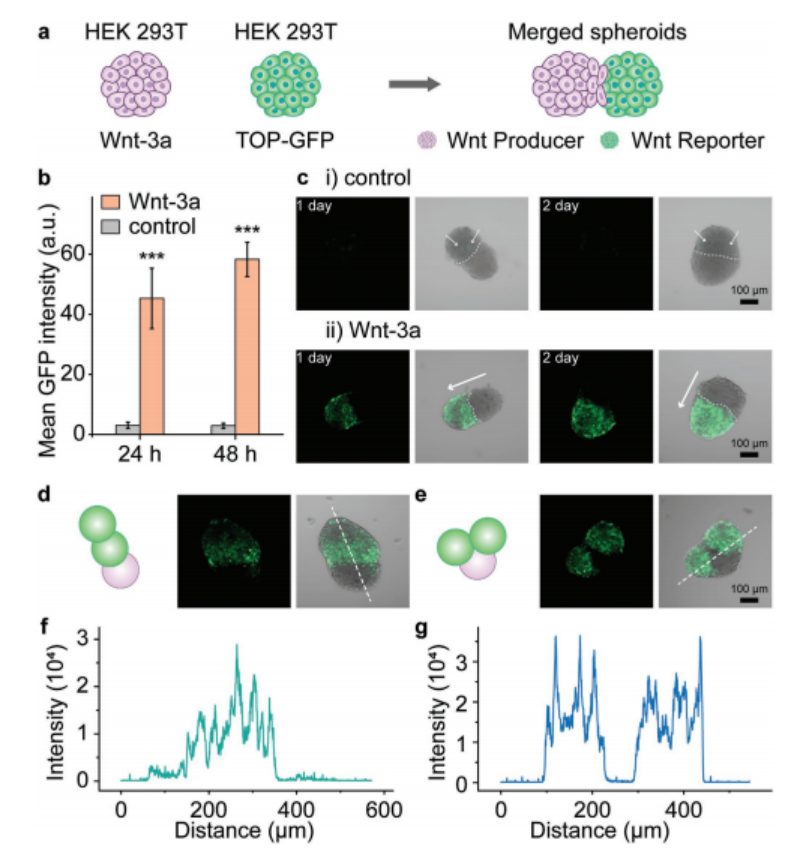
圖5. 合并球體之間的Wnt信號。a)由產生球體(HEK 293T、Wnt-3a)和報告球體(HEK 293T、TOP-GFP)組成的多球體復合物構成的Wnt信號傳播系統示意圖。b)報告球體激活圖。通過共聚焦圖像中GFP熒光的強度來估計激活。(GFP強度由至少10個合并的球體計算。***, P < 0.001,單因素方差分析)c)共聚焦圖像顯示GFP熒光估計報告球體中Wnt/β-catenin信號的激活。i) HEK 293T球體(對照)和報告球體的合并球體。白色箭頭指向微弱的GFP熒光。ii)一個Wnt產生球(HEK 293T)和一個Wnt報告球(HEK 293T, TOP-GFP)的合并球。白色箭頭指向Wnt傳播方向。d,e)所研究的兩個三重球體的示意圖和熒光顯微鏡圖像,其中一個Wnt產生球體(HEK 293T)和兩個Wnt報告球體(HEK 293T, TOP-GFP)。f)如圖(d)所示三重球體白色虛線上GFP熒光強度分布圖。g)如圖(e)所示三重球體白色虛線上GFP熒光強度分布圖。
本文通過proMAD方法成功實現了多個同型或異型球體的融合,形成了雙球體、多球體和異質球體等各種多球體結構,并確定了不同結構的組合概率。與現有的3D細胞培養方法相比,proMAD方法具有諸多獨特優勢。如高通量、小型化、已操作及快速形成復雜多極結構等。I-DOT在前期球體的制備過程中保證了每個液滴的準確性,間接影響了最終多球體結構的形成。同時,該方法也為研究3D細胞培養模型中的細胞信號傳導提供了強大工具,I-DOT在多個關鍵步驟中發揮重要作用的同時,更有助于在更接近生理條件下研究各種生物學過程,為組織工程和再生醫學的發展提供新的思路和方法。
同騰睿杰(上海)生物技有限公司作為CYTENA I.DOT中國總代理商,為您提供優質的售前售后服務。
聯系電話:021-50826962
聯系郵箱:sales@ttbiotech.com




